El 14 de noviembre 2013 se ha dictaminado, por una corte francesa, el fallo judicial por el que una firma alemana, encargada de establecer estándares de seguridad, deberá pagar una compensación multimillonaria a centenares de mujeres que fueron operadas con implantes mamarios defectuosos.
La empresa en cuestión, TUV RHEINLAND, es una entidad líder en servicios técnicos a nivel mundial. Fue fundada ya en el lejano 1872 y tiene, a día de hoy, oficinas repartidas en 65 países. La idea clave u objetivo final de la actividad empresarial de TUV RHEINLAND es, y decimos “supuestamente” vista la disonancia cognitiva entre lo que debería ser y lo que realmente es, “el desarrollo sostenible de la Seguridad y Calidad en las interacciones entre el hombre, la tecnología y el medioambiente”. Así se afirma en la misma página web de la susodicha. Por ello, afirman que su dedicación va dirigida a dar asistencia técnica, promover, inspeccionar, ensayar, auditar y certificar en ciertos ámbitos de actuación u áreas de negocio, entre las cuales, destaca, a interés de la noticia analizada, “Salud y Bienestar, Gestión de Suministros en el Sector Sanitario”.
En concreto, la empresa notificadora descrita otorgó Certificados de Seguridad Europeos a una firma francesa dedicada a producir prótesis para implantes mamarios.
Los hechos, los que se describen a continuación. Se descubrió que la silicona utilizada para producir los implantes era de una calidad sub-estándar lo que conllevó a que éstos fueran propensos a rupturas, fugas, explosiones e incomodidades. Es decir, no eran prótesis aptas para el uso sanitario. (Lo cual ya nos da a entender que antes de la distribución del producto éste era catalogable de defectuoso, lo cual implica ya hablar de repartición posiblemente solidaria de la responsabilidad por los daños producidos al consumidor final. Cuestión ésta que en cualquier caso analizaremos más adelante ya que nos encontramos en un entramado no fácil de responsabilidad múltiple.)
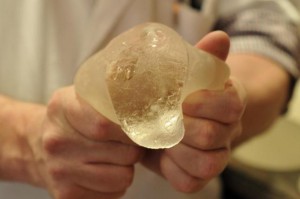
Fabricadas las prótesis, como producto defectuoso, éstas se han distribuido, mediante la ya conocida dinámica “fabricante-distribuidor-proveedor” de una forma tan extensiva que el número de afectadas ha llegado a ser de 1.700 mujeres/demandantes. Número que podría llegar a ser incluso mayor si no tuviéramos en cuenta el dúo “afectada-demandante”, sino únicamente “usuaria”. Las afectadas que han decidido interponer demanda judicial están dirigiendo la misma a la compañía alemana o notificadora encargada de distribuir los certificados europeos ya que se considera que una simple inspección somera del producto debería haber identificado el problema del mismo. Al respecto, lo que posiblemente extraña es que la demanda se haya dirigido con carácter exclusivo a la empresa notificadora…
Ahora bien, independientemente del fallo judicial dirigido a la empresa alemana, ya en mayo de 2013, los fiscales del juicio, y no los demandantes, pedían une pena de cárcel 4 años para el fabricante, Jean-Claude Mas, fundador de la empresa POLY IMPLANT PROTHÉSE (PIP) acusándolo de haber vendido cientos de miles de implantes mamarios defectuosos. Es decir, al fabricante, por lo que ya empezamos a ver como la responsabilidad se distribuye entre empresa notificadora y fabricante. A nuestro juicio, existen incluso otros responsables que a continuación detallaremos. La acusación habla de fraude agravado por el uso de silicona de baja calidad, multa e inhabilitación en el ámbito médico y empresarial, estafa civil y responsabilidad contractual.
Los problemas que se sustancian ante los hechos descritos abarcan distintos ámbitos que analizaremos de forma somera.
En primer lugar, hacemos referencia a la problemática que ello suscita a nivel europeo y, por tanto, la normativa europea, con el sistema de funcionamiento y concesión de la Marca Europea y la posible falta de transparencia y de mínimo común denominador entre las empresas notificadoras.
En segundo lugar, con referencia a la normativa española inclusive y los distintos tipos de responsabilidad exigible, así como a la distinción en cuanto a la negligencia o diligencia médica con respecto a las obligaciones de medios y de resultados. Y obviamente responsabilidad solidaria entre fabricante, distribuidor y proveedor.
En primer lugar, a nivel europeo numerosas son las críticas dirigidas a la actuación de la Comisión Europea a la cual se acusa de no estar actuando con la suficiente rapidez para la protección de los pacientes posiblemente afectados por los implantes médicos. Lo cual es lo mismo a decir falta de protección del usuario o consumidor final en un ámbito que merece particular atención como es el sanitario independientemente del tipo de obligación de medio o de resultado al que se haga referencia.
Ante todo la regulación o, mejor dicho, la actualización de las regulaciones sectoriales se está realizando de forma paulatina. Al efecto, se prevén que los cambios tendrán efecto no antes de 2015. En palabras de Andrew Miller, Presidente del Comité Selecto de Ciencia y Tecnología del parlamento británico “Creo que por el bien de los pacientes podríamos poner en práctica un mejor sistema si la Comisión acelerará el proceso de revisión de las actuales regulaciones”.
El actual sistema de concesión de la Marca CE o Marca de Conformidad representa, en pocas palabras o hablando en plata, “el testimonio por parte del fabricante de que su producto cumple con los mínimos requisitos legales y técnicos en materia de seguridad” aunque, se dice, que ello no implica la calidad del producto. Esto es a mi juicio lo que se llama una disonancia cognitiva aplicada al ámbito material.
Ello implica que si el producto supera o cumple con los supuestos requisitos o con las provisiones de las Directivas Europeas aplicables, el producto en cuestión puede entrar en el mercado sin que ningún EM pueda prohibir su entrada. Otra disonancia cognitiva ya que si se parte del presupuesto, como afirman las entidades públicas o autoridades, que no necesariamente los certificados de seguridad representan, en todos los ámbitos de concesión y con la actual regulación, calidad del producto es absurdo pensar que no pueda haber controles estatales superiores que prohíban la entrada del producto si éste no supera controles múltiples.
El problema es que la Marca CE solo se limita a afirmar que el producto entra en el mercado habiendo cumplido todos los requisitos legales esenciales como requisitos de seguridad, de salud o protección medioambiental. (Por lo menos es lo que se dice).
Los requisitos deberían representar un mínimo común denominador que debería ser gestionado de manera uniforme por parte de las distintas empresas notificadoras que, al parecer, no se está gestionando con la misma eficiencia o mismo procedimiento. Lo cual plantea el problema de que los fabricantes acudan a ciertos organismos menos estrictos. Además de la posibilidad de que los organismos notificadores confíen en información de seguridad reunida para productos similares o equivalentes sin someter el implante en cuestión a pruebas de seguridad específicas. Existe una falta de calidad y de seguridad en el procedimiento de concesión de la Marca y, obviamente, en el actuar de las empresas notificadoras.
En segundo lugar, dejando al margen la ineficaz regulación europea y la gestión procedimental del mecanismo,otras preguntas son las siguientes, ¿hasta qué punto podemos imputar a un médico la falta de diligencia en el uso u aplicación de dichas prótesis de conformidad con la lex artis? ¿Cómo podemos eludir la responsabilidad médica ante un material que forma directamente parte de los conocimientos mínimos y necesarios en la prestación del servicio médico? ¿No podemos exigir a un médico que informe de manera obligatoria de cualquier falla que encuentre en un producto? ¿Tiene obligación el profesional de conocer a la perfección el material quirúrgico que está utilizando o puede eximirse de dicho conocimiento haciendo recaer la responsabilidad en unos certificados que han demostrado no funcionar? Lo cual implica preguntar si podemos exigir y hasta qué punto?
Desde el mismo sector sanitario, en particular modo el profesor Norman Williams, presidente del Colegio Real de Cirujanos del Reino Unido, se aclama urgentemente “un incremento en la transparencia y responsabilidad de todo el marco encargado de regular los implantes médicos“. Pero…¿responsabilidad también de quién?
“Existe una necesidad urgente de más transparencia en el sistema regulador para que los pacientes y los médicos conozcan la procedencia del implante y, lo más crucial, si el producto previamente ha sido rechazado por otros organismos reguladores” expresa el señor Miller, Presidente del Comité Selecto de Ciencia y Tecnología del parlamento británico.
Esas afirmaciones con respecto a la extensión y la búsqueda de un mayor grado de responsabilidad nos conllevan al planteamiento doctrinal y jurisprudencial que vierte sobre la responsabilidad médica y, en particular modo, a las obligaciones de medio y las de resultado y las diferencias en cuanto a la diligencia médica y la responsabilidad objetiva.
La posibilidad de exigir responsabilidad médica al facultativo suele distinguirse, pese a la existencia de distintas corrientes doctrinales o corrientes jurisprudenciales, en primer lugar, en cuanto al tipo de prestación médica que se suele prestar o a la que se somete el paciente.
Por ello, se distingue entre medicina necesaria y medicina voluntaria. Con respecto a ello citamos como criterio reiterado del TS “que la obligación del médico y, en general, del profesional sanitario, no es la de obtener en todo caso una recuperación del enfermo, o lo que es igual, no es la suya una obligación de resultado sino de medios, es decir, está obligado no a curar el enfermo, sino a proporcionarle todos los cuidados que requiera según el estado de la ciencia; además, en la conducta de los profesionales sanitarios queda descartada la responsabilidad objetiva, ya que a la relación causal ha de sumarse ese reproche culpabilístico”. (STS 24 de enero de 2007)
En la medicina necesaria, se suele imputar la responsabilidad al facultativo solo en cuanto éste no haya actuado de conformidad con la lex artis y, por tanto, si su actuación no se conforma con la diligencia esperada en su ámbito de actuación. Y, obviamente, siempre y cuando, existan como requisitos necesarios los siguientes: daño antijurídico, patrimonial o moral, relación de causalidad y culpa o negligencia médica.
Con carácter general podemos afirmar que en cuanto a la jurisprudencia respecta existen ciertos criterios generales de aplicación que implican:
– Rechazo de responsabilidad objetiva (STS 31 de enero de 2003)
– Distinción entre obligaciones de medio (medicina curativa o necesaria) y de resultado (medicina voluntaria o satisfactiva – STS 24 de enero de 2007)
– Carga de la prueba a la victima
Sin embargo, en la medicina voluntaria se imputa la responsabilidad al facultativo en base a la no consecución del resultado esperado independientemente de que su actuar profesional este de conformidad con la lex artis. Por ejemplo, en el caso de una operación estética de pecho el paciente ya contrata con el médico un determinado resultado final de la prestación que, en caso de no ser conseguido, es totalmente reclamable.
Con respecto a ello, en el caso que nos interesa, la pregunta es si podemos exigir responsabilidad al facultativo cuya obligación es prestar un resultado final y que éste no se consigue por un defecto en el implante. Es decir, ¿el implante defectuoso puede subsumirse a la reclamación que abarca la no consecución del resultado contratado? Por tanto, ¿es deber del médico conocer la calidad y la seguridad del material que está usando en su prestación médica? Nos encontramos ante un ¿responsabilidad contractual o extra-contractual? ¿Podemos demandar también al médico? Existe una responsabilidad solidaria? ¿Que alcance tiene la responsabilidad derivada de bienes o productos defectuosos?
A mi juicio, es totalmente exigible la responsabilidad al facultativo en el ámbito de una obligación de resultado como el aumento de pecho cuyo resultado ha fracasado debido a un defecto en el implante o en el material quirúrgico. Al efecto, al analizar la Sentencia del Tribunal Supremo 766/1999 de 24 de septiembre encontramos una total identidad de razón que nos permite aplicar los mismos fundamentos de derecho al caso analizado.
En estos casos, no sirve de excusa exculpatoria “agarrarse” a conceptos como el consentimiento informado prestado por el paciente. Ya que existen estudios de carácter internacional que demuestran que hay una fuerte tendencia a considerar el consentimiento informado como una herramienta que protege a los proveedores de salud de posibles problemas legales y futuros reclamos en lugar de considerar simplemente el consentimiento informado como un proceso de decisión en el que actúan capacidad, voluntariedad, información y comprensión pero en ningún caso el deber de soportar un daño antijurídico, patrimonial o moral!
Existen corrientes doctrinales que se plantean calificar, además, la actividad médica como una actividad de riesgo; otras que hablan de riesgo permitido socialmente o ilicitud generalmente inconsciente. ¿Es posible aplicar la teoría del riesgo? En pocas palabras, hay material para debatir.